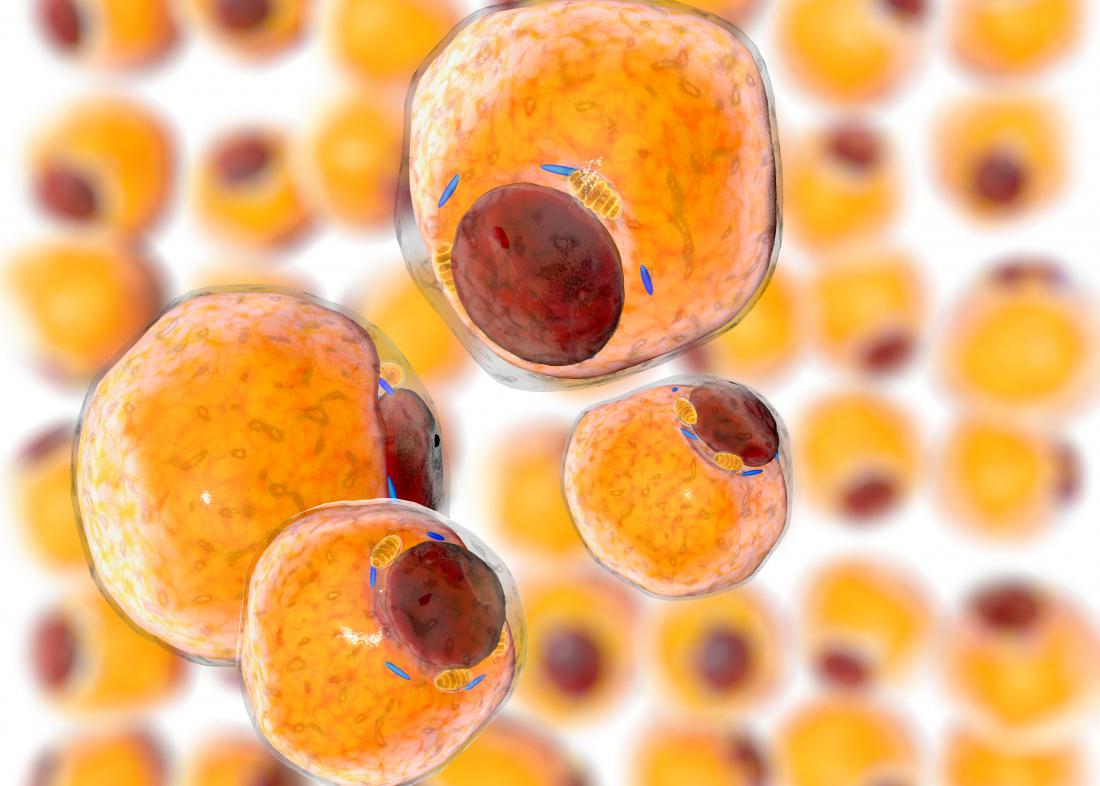
Komórki nowotworowe nieustannie rosną i dzielą się, co oznacza, że potrzebują stałego zaopatrzenia w energię. Nowe badania analizują, w jaki sposób rak czerpie paliwo z komórek tłuszczowych, a także odkrywają potencjalny mechanizm, który może zagłodzić guz w jego odżywianiu.
Rak to coraz bardziej złożony temat badań, w którym każdy dostrzegalny kąt natarcia jest analizowany przez badaczy. Pomimo milionów godzin eksperymentów, wciąż pozostaje wiele pytań bez odpowiedzi.
Z każdym nowym odkryciem staje się coraz bardziej oczywiste, że rak należy postrzegać jako chorobę całego ciała. Aby nowotwór mógł przeżyć i dobrze się rozwijać, musi czerpać energię z komórek i tkanek, wykorzystywać układ krążenia oraz unikać detekcji przez układ odpornościowy. Nowotwory muszą więc prowadzić inteligentną grę, aby utrzymać swój wzrost i integrować się z organizmem.
Naukowcy skupiają się teraz na atakowaniu nie tylko komórek nowotworowych, ale także na systemach, na których opierają się guzy, aby je podtrzymać.
Guz, metabolizm i tłuszcz
Zespół badawczy z Sanford Prebys Medical Discovery Institute w San Diego w Kalifornii szczególnie interesuje się tym, jak nowotwory komunikują się z komórkami tłuszczowymi. Współautorka badań, Maria Diaz-Meco, podkreśla, że «musimy rozważyć inne aspekty terapii przeciwnowotworowej wykraczające poza bardziej znaną genetykę. Oznacza to, że powinniśmy inwestować w badania nad metabolizmem nowotworów, które identyfikują podatności, mające zastosowanie do wszystkich rodzajów nowotworów.»
Ta linia badań jest kluczowa. Jak kontynuuje Diaz-Meco: «To ostatecznie doprowadzi do lepszych terapii, które będą mniej podatne na opór, co jest zbyt powszechnym problemem w podejściu do terapii celowanej na onkogeny.»
W Stanach Zjednoczonych rak prostaty jest drugą najczęstszą przyczyną zgonów związanych z rakiem u mężczyzn. Otyłość uznawana jest za główny czynnik ryzyka, która przewiduje, jak agresywnie może zachowywać się rak. Jednak dokładny mechanizm, w jaki otyłość wpływa na wyniki leczenia raka prostaty, wciąż pozostaje niejasny.
Dotychczasowe badania nad otyłością a rakiem prostaty koncentrowały się głównie na myszach, które były karmione dietą wysokotłuszczową. Starszy autor badań, Jorge Moscat, wyjaśnia, dlaczego takie podejście nie jest idealne.
«Choć naśladuje to niektóre sytuacje u pacjentów, uniemożliwia to prawdziwe zrozumienie ścieżek sygnałowych, które kontrolują dwukierunkową komunikację między guzami a adipocytami, czyli komórkami tłuszczowymi.»
«To jest niezbędne,» dodaje Moscat, «jeśli chcemy zidentyfikować cele terapeutyczne, które mogą być wykorzystane do zapobiegania sygnałom pro-nowotworowym pochodzącym z tkanki tłuszczowej.»
Moscat i Diaz-Meco podeszli do tego problemu z nowego kierunku, wykorzystując model myszy pozbawionego białka znanego jako p62 w komórkach tłuszczowych. Myszy z niedoborem tego białka stają się otyłe, nawet przy standardowej diecie.
Ich intrygujące wyniki zostały opublikowane w czasopiśmie.
Guzy wykorzystują komórki tłuszczowe do paliwa
Naukowcy odkryli, że p62 odgrywa kluczową rolę w komunikacji między tkanką tłuszczową a nowotworami. Białko to wspomaga «kondycję metaboliczną» raka, sprzyjając jego progresji i metastazie. Działa to poprzez hamowanie drugiego białka, znanego jako mTORC1.
Kiedy mTORC1 jest tłumiony, hamowane są również energochłonne procesy komórek tłuszczowych, takie jak oksydacyjna fosforylacja oraz «metabolizm kwasów tłuszczowych w białej tkance tłuszczowej». Dzięki zatrzymaniu tych procesów dostępnych jest więcej kwasów tłuszczowych i innych składników odżywczych, które nowotwór może wykorzystać do wzrostu i rozwoju.
«Metaboliczne przeprogramowywanie wynikające z utraty p62 w adipocytach wydaje się pomagać nowotworom radzić sobie z wysokimi wymaganiami energetycznymi agresywnego raka,» stwierdza Maria Diaz-Meco, Ph.D.
W dalszych eksperymentach zespół wykazał, że brak p62 promuje także wytwarzanie Cpt1a i osteopontyny, które wspierają proliferację komórek nowotworowych i ich przerzuty.
W szczególnie agresywnym, opornym na kastrację raku prostaty, stwierdzono wyższe stężenia Cpt1a i osteopontyny.
Te ustalenia mają ogromne znaczenie dla przyszłych metod leczenia raka. Jak mówi Moscat: «Znaczenie jest ogromne, ponieważ identyfikujemy nowy zestaw celów terapeutycznych, które, jeśli zostaną zmodulowane, powinny blokować zdolność aktywowanej tkanki tłuszczowej do promowania nowotworów złośliwych.»
Obecnie inhibitory mTOR są stosowane w leczeniu wielu nowotworów. Naukowcy mają obawy, że mogą one zablokować metabolizm tkanki tłuszczowej, co może w niektórych przypadkach przyczynić się do wzrostu guza.
Niemniej jednak konieczne będą dalsze badania, aby potwierdzić, czy tak rzeczywiście jest.
Nowe Odkrycia i Perspektywy na Przyszłość
W miarę jak badania nad interakcjami między komórkami tłuszczowymi a nowotworami postępują, zyskujemy coraz więcej informacji, które mogą prowadzić do rewolucyjnych zmian w terapii nowotworowej. Najnowsze badania wskazują, że zrozumienie metabolizmu komórek tłuszczowych i ich wpływu na nowotwory może stać się kluczem do opracowania nowych strategii terapeutycznych. Na przykład, badania wykazały, że manipulacja poziomem p62 w adipocytach może znacząco wpłynąć na rozwój nowotworów.
Podobnie, nowe terapie celujące w mTORC1 mogą nie tylko zmieniać metabolizm nowotworów, ale także poprawiać wyniki pacjentów z rakiem prostaty. Naukowcy badali różne podejścia, aby optymalizować skuteczność tych terapii, jednocześnie minimalizując ryzyko wystąpienia oporności. Takie innowacje mogą zrewolucjonizować sposób, w jaki podchodzimy do leczenia nowotworów w przyszłości.
Przyszłość wygląda obiecująco, a badania w tej dziedzinie mogą przynieść nadzieję wielu pacjentom. Ważne jest, aby kontynuować poszukiwania i rozwijać nowe metody, które mogą w końcu prowadzić do skuteczniejszego leczenia i lepszej jakości życia dla osób dotkniętych rakiem.