Jeśli myśl o przejściu pod nożem napełnia cię strachem, uspokój się. Operacja nie jest już brutalnym i niebezpiecznym doświadczeniem, przed jakim stają nasi przodkowie. Dzięki cudom takim jak laparoskopia, rozwiązania robotyczne, a ostatnio także iKnife i laserowa sonda, interwencja chirurgiczna staje się coraz bezpieczniejsza.
Archeolodzy uważają, że ludzie przeprowadzają operację nawet przez 11 000 lat. Operacja czaszkowa, znana jako trepanacja, prawdopodobnie pochodzi z epoki neolitu. Wymagało to wywiercenia dziury w czaszce żywej osoby.
Spekulacja sugeruje, że zrobiono to, aby wyleczyć zaburzenia, takie jak konwulsje, złamania, bóle głowy i infekcje. Starożytni Egipcjanie stosowali tę samą operację do «wypuszczania» bólów głowy i migreny.
Od 1812 r. Oferty opisują procedury, które teraz można uznać za makabryczne, takie jak przekazanie haka przez źrenicę ucznia podczas usuwania zaćmy i używanie pijawek do upuszczania krwi. Pionierzy swoich czasów, zarówno chirurdzy, jak i pacjenci odznaczali się niezwykłą odwagą.
Przeskocz stamtąd do teraźniejszości, a ty masz minimalnie inwazyjną operację, w której nawet przeszczep serca jest obecnie stosunkowo rutynowy. Według United Network for Organ Sharing (UNOS) od stycznia 1988 r. do lipca 2016 r. w Stanach Zjednoczonych przeprowadzono 64 055 transplantacji serca.
Postępy w chirurgii minimalnie inwazyjnej
W 1987 r. francuski ginekolog przeprowadził pierwszą rozpoznaną operację laparoskopową w celu usunięcia pęcherzyka żółciowego. Stamtąd praktyka szybko się rozszerzyła. Według amerykańskiej Agencji ds. Żywności i Leków (FDA) każdego roku w Stanach Zjednoczonych przeprowadza się ponad 2 miliony operacji laparoskopowych.
W chirurgii laparoskopowej lub «dziurka» mała rurka ze źródłem światła i kamerą przechodzi przez ciało, aż dotrze do odpowiedniej części. Obszary, które wymagają obsługi, pojawiają się na ekranie, podczas gdy chirurg używa narzędzi przez małe otwory.
Procedury małoinwazyjne oznaczają mniejsze nacięcia z mniejszymi bliznami, mniejsze ryzyko infekcji, krótsze pobyty w szpitalu i zmniejszoną rekonwalescencję.
Roboty chirurgiczne
Następny przystanek, robotyka. W 2000 r. zespół naukowców w Niemczech, którzy badali techniki minimalnie inwazyjnej chirurgii, ogłosił, że opracowali system z dwoma robotycznymi ramionami, które są kontrolowane przez chirurga na konsoli sterującej. Nazwali to ARTEMIS.
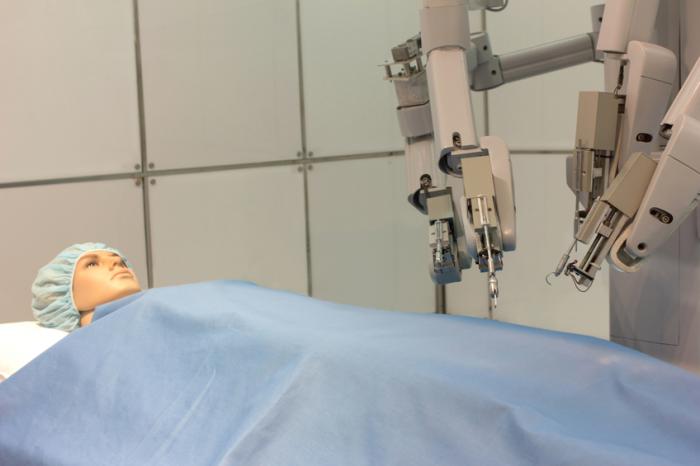
W lipcu 2000 r. system da Vinci został zatwierdzony do użytku w USA w celu cięcia i operacji.
Był to pierwszy zrobotyzowany system chirurgiczny, który uzyskał aprobatę FDA, a jego użycie stało się stosunkowo powszechne.
System składa się z trzech elementów: wózka do wizji ze źródłem światła i kamerami, konsoli głównej, w której siedzi chirurg, oraz ruchomego wózka z dwoma ramionami instrumentu i ramieniem kamery.
Kamera zapewnia prawdziwy trójwymiarowy obraz, który jest wyświetlany nad rękami chirurga, więc końcówki instrumentów wydają się być przedłużeniem uchwytów sterujących. Pedały sterują elektrokoagulacją, ogniskowaniem kamery, sprzęgłami ramion instrumentów i kamer oraz głównymi uchwytami sterującymi, które kierują robotycznymi ramionami pacjenta po stronie pacjenta.
Pojawiły się doniesienia o błędach i błędach, niektóre z nich były śmiertelne i nie wszyscy są przekonani, że roboty chirurgiczne naprawdę dają lepsze wyniki leczenia.
Czego oko nie widzi
Nóż elektrochirurgiczny został wynaleziony w latach dwudziestych XX wieku. Za pomocą prądu elektrycznego szybko nagrzewa tkankę ciała, umożliwiając chirurgowi przebicie tkanki przy minimalnej utracie krwi. Jest powszechnie stosowany w chirurgii onkologicznej.
Operacje obrazowe, takie jak laparoskopia, zmniejszyły zakres interwencji w wielu operacjach.
Jednakże, jeśli chodzi o raka, obrazy mogą pokazać, gdzie znajduje się guz, ale ani obrazy, ani ludzkie oko nie mogą łatwo odróżnić zdrowych od niezdrowych tkanek.
Dr Zoltan Takats, z Imperial College London w Wielkiej Brytanii, zobaczył sposób, w jaki nóż elektrochirurgiczny wypełnia lukę, której obrazy nie potrafią.
Wejdź do iKnife. Oparty na elektrochirurgii, iKnife potrafi dokładnie wykryć, które tkanki wymagają usunięcia, a które powinny pozostać.
Do niedawna jedynym definitywnym sposobem ustalenia, czy tkanka jest nowotworowa czy nie, było pobranie biopsji do badania, zwykle pod mikroskopem. Wadą jest to, że podczas zabiegu można pobrać i przetestować tylko bardzo niewiele próbek, a wykonanie każdego testu może zająć 40 minut. Nie jest to praktyczny sposób określenia krawędzi guza podczas operacji.
W 2013 r. pojawił się pierwszy nóż, który umożliwia chirurgowi zbadanie tkanki biologicznej poprzez powiązanie elektrochirurgii ze spektrometrią mas. W spektrometrii mas, zjonizowanych lub naładowanych cząstki przepuszczane są przez pola elektryczne lub magnetyczne.
Spektrometria masowa umożliwia pomiar stosunku masy do ładunku, a pomiary te umożliwiają rozróżnienie tkanek o różnym składzie, znanych jako profilowanie chemiczne. Analizując skład chemiczny różnych próbek, można stwierdzić, które tkanki są zdrowe, a które nie.
W tym czasie dr Takats powiedział, że spodziewa się, że iKnife będzie miał zastosowanie w różnych rodzajach operacji i że obniży koszty.
Jak działa iKnife
Cięcie za pomocą elektroskalpelów powoduje, że tkanka ulega odparowaniu podczas cięcia. W ten sposób powstaje dym, który normalnie jest zasysany przez systemy wyciągowe. Ale podłączając iKnife do spektrometru masowego i pompując dym w jego kierunku, para może zostać «przechwycona» i przeanalizowana pod kątem składu chemicznego. Po dopasowaniu wyników do biblioteki referencyjnej chirurg może zobaczyć, który rodzaj tkanki znajduje się w ciągu 3 sekund.
W 2013 r. dr Takats i jego zespół użyli iKnife do analizy próbek tkanek pobranych od 302 pacjentów, którzy przeszli operację usunięcia różnych rodzajów nowotworów, zarówno nowotworowych, jak i nienowotworowych.
Zapisali charakterystykę tysięcy próbek tkanek pobranych z guzów mózgu, płuc, piersi, żołądka, okrężnicy i wątroby. Na podstawie tych próbek utworzyli bazę danych zawierającą 1624 rakowate i 1309 nie-rakowych zapisów, do których można dobrać przyszłe próbki.
Następnie zespół zastosował iKnife z szybką spektrometrią masową z jonizacją wyparną (REIMS) w 81 interwencjach chirurgicznych. Podczas operacji wykonywano odczyty, a tkankę testowano później w konwencjonalny sposób. W każdym przypadku odczyt dokładnie zgadzał się z pooperacyjną diagnozą histologiczną.
iKnife został opracowany do elektrochirurgii, ponieważ chirurdzy dostrzegli jego potencjał do usuwania guzów nowotworowych, ale jego zastosowanie do chirurgii wodnej i laserowej zostało już podniesione. W przyszłości może być stosowany do odczytywania w celu analizy błon śluzowych i układu oddechowego, moczowo-płciowego lub żołądkowo-jelitowego.
Urządzenie iKnife jest już używane w Imperial College London i obecnie jest testowane w chirurgii raka piersi, okrężnicy i jajnika.
Laserowe wykrywanie guzów mózgu
Niedawno badacze w Wielkiej Brytanii i Kanadzie powiązali urządzenie iKnife z sondą laserową w celu wykrycia nieprawidłowej tkanki podczas zabiegu chirurgicznego w celu usunięcia guza mózgu.
W tej technice wykorzystano sondę laserową w bliskiej podczerwieni, aby określić, czy tkanka była rakowa czy zdrowa, mierząc światło odbite od tkanki.
Szybkie fakty dotyczące postępów w chirurgii
- Pierwsze udane zastosowanie znieczulenia eterowego nastąpiło w 1846 roku
- Kwas karbolowy został po raz pierwszy użyty jako środek antyseptyczny w latach 1867-1876
- W 1907 r. powstał pierwszy sztuczny antybiotyk.
Kiedy skierowali wiązkę światła na odsłonięty mózg, cząsteczki w komórkach zaczęły wibrować. Kiedy to zrobili, światłowód w sondzie zbierał rozproszone światło, które odbijało się od tkanki.
Mierząc częstotliwość wibracji, naukowcy byli w stanie stwierdzić, która tkanka była zdrowa, a która nie. Podobnie jak w przypadku iKnife analiza trwała zaledwie kilka sekund.
W chirurgii onkologicznej umiejętność wykrycia dokładnej granicy obszaru tkanki nowotworowej może sprawić, że różnica między życiem a śmiercią oraz między koniecznością powtórzenia operacji lub nie.
Zdolność do usunięcia dokładnej tkanki nie tylko zapewnia usunięcie całego guza, ale także zmniejsza niepotrzebną utratę tkanki, prowadząc do lepszych wyników dla pacjentów.
Naukowcy zauważają, że szczególnie w przypadku guzów mózgu niezdolność widzenia granicy guza, nawet przy użyciu mikroskopu chirurgicznego, naraża ludzi na dodatkowe ryzyko uszkodzenia, takie jak utrata mowy. Wraz z postępem technologii ryzyko operacji zmniejsza się stopniowo.