Nowe badania dają nadzieję na innowacyjne leczenie pacjentów z glejakiem, po zidentyfikowaniu sposobu na powstrzymanie rozwoju tego zagrażającego życiu nowotworu mózgu.
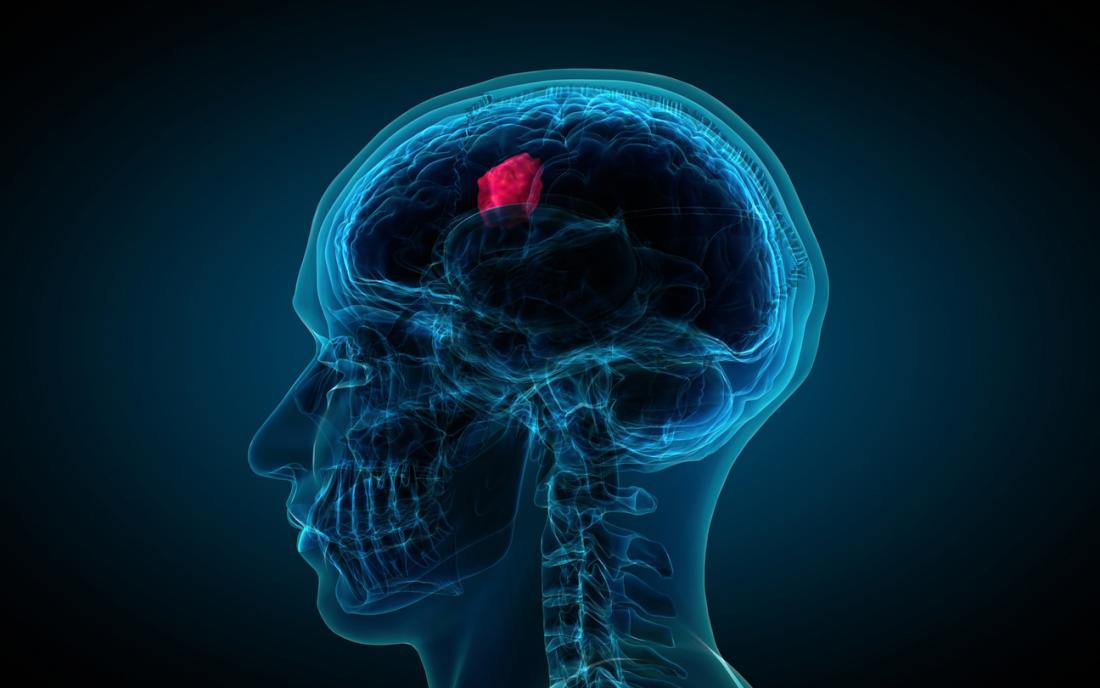
Naukowcy z Massachusetts Institute of Technology (MIT) w Bostonie zidentyfikowali mechanizm, dzięki któremu określone białko zwane PRMT5 stymuluje wzrost guzów glejaka.
Co więcej, blokując ten mechanizm za pomocą klasy istniejących leków, byli w stanie zatrzymać wzrost nowotworu glioblastoma u myszy.
Kierownik badania, Christian Braun, który był doktorantem w MIT w czasie badań, oraz jego koledzy niedawno opublikowali swoje wyniki w prestiżowym czasopiśmie.
Glejak, zwany także glejakiem wielopostaciowym, jest nowotworem złośliwym mózgu, który rozwija się z gwiazdotwórczych komórek glejowych, zwanych astrocytami.
Według American Brain Tumor Association, w tym roku w Stanach Zjednoczonych zostanie zdiagnozowanych blisko 80 000 nowych przypadków pierwotnych guzów mózgu. Spośród nich glejak wyniesie około 14,9 procent.
Chociaż glejak nie jest najczęstszym nowotworem mózgu, jego złośliwość czyni go jednym z najbardziej niebezpiecznych; mediana przeżycia wynosi zaledwie 14,6 miesiąca po rozpoznaniu glioblastoma, jeśli pacjent jest leczony chemioterapią i radioterapią.
W związku z tym istnieje pilna potrzeba opracowania nowych terapii, które mogą skutecznie zapobiegać i leczyć glioblastoma. Braun i jego współpracownicy są przekonani, że wyniki ich badań mogą przyczynić się do osiągnięcia tego celu.
PRMT5 i Splatanie Genów
W poprzednich badaniach Braun oraz jego koleżanka Monica Stanciu z Departamentu Biologii w MIT zidentyfikowali PRMT5 jako potencjalny czynnik wywołujący nowotwory glejaka, jednak dokładne mechanizmy, za pomocą których białko to działa, pozostawały niejasne.
Odkrycia wskazują, że PRMT5 może uczestniczyć w unikalnym procesie «splicingu genów», który napędza wzrost glejaków.
Naukowcy wyjaśniają, że składanie genów to proces, w którym odcinki informacyjnego RNA (mRNA) zwane intronami są «wycinane» z nici mRNA, ponieważ nie są już potrzebne po przekazaniu informacji genetycznej.
Późniejsze badania ujawniły, że około jeden do trzech «zatrzymanych intronów» utrzymuje się w około 10 do 15 procent ludzkich nici mRNA, a te pozostałe introny zapobiegają opuszczaniu jądra komórkowego przez cząsteczki mRNA.
«Uważamy, że te nici są w zasadzie zbiornikiem mRNA» – mówi Braun, który obecnie pracuje w Ludwig Maximilian University of Munich w Niemczech. «Macie te bezproduktywne izoformy w jądrze, a jedyną rzeczą, która powstrzymuje ich przed tłumaczeniem, jest ten jeden intron».
W swoich najnowszych badaniach, jak postawiono hipotezę, naukowcy odkryli, że PRMT5 odgrywa kluczową rolę w unikalnym procesie składania genu; sugerują, że komórki macierzyste mózgu mają wysoki poziom PRMT5, którego używają do efektywnego składania i zwiększonej ekspresji genów związanych z proliferacją komórek, czyli wzrostem i dzieleniem.
«Gdy komórki zbliżają się do dojrzałego stanu, poziomy PRMT5 spadają, zatrzymywane poziomy intronów rosną, a te informacyjne RNA związane z proliferacją utknęły w jądrze» – wyjaśnia współautorka badania Jacqueline Lees z Instytutu Integratywności Davida H. Kocha Cancer Research at MIT.
Eksperci zauważają, że w rakowych komórkach mózgowych poziom PRMT5 wzrasta jeszcze raz, co z kolei aktywuje unikalny proces splatania genów i zachęca komórki nowotworowe do wymknięcia się spod kontroli.
Hamowanie Wzrostu Glejaka u Myszy
Naukowcy potwierdzili następnie swoje odkrycia w ludzkich komórkach glejaka. Kiedy zahamowali PRMT5 – który zapobiega wytwarzaniu białka PRMT5 – w komórkach nowotworowych, odkryli, że wzrost i podział komórek został zatrzymany.
Naukowcy byli również w stanie powstrzymać wzrost guzów glejaka w modelach myszy, stosując inhibitory PRMT5.
Omawiając odkrycia zespołu, Omar Abdel-Wahab z Memorial Sloan Kettering Cancer Center w Nowym Jorku – który nie był zaangażowany w badania – mówi: «PRMT5 ma wiele ról i do tej pory nie było jasne, jaka droga jest naprawdę ważna ze względu na jej wpływ na raka.»
«To, co znaleźli,» dodaje, «to że jednym z kluczowych czynników jest mechanizm składania RNA, a ponadto, gdy splicing RNA zostaje przerwany, ta kluczowa ścieżka jest wyłączona.»
Dodatkowo w badaniu zidentyfikowano biomarker, który według naukowców może być użyty do identyfikacji pacjentów, którzy mogą dobrze reagować na leczenie inhibitorami PRMT5.
To badanie rzuca światło nie tylko na podstawowe przyczyny glejaka, ale także może otworzyć drzwi do nowych strategii zapobiegania i leczenia tego śmiertelnego nowotworu.
Nowe Perspektywy Terapeutyczne
Rok 2024 przynosi nowe nadzieje dla pacjentów z glejakiem, ponieważ badania nad PRMT5 i innymi mechanizmami molekularnymi przynoszą obiecujące wyniki. W ostatnich badaniach zidentyfikowano inne potencjalne cele terapeutyczne, które mogą wspierać tradycyjne metody leczenia, a także wprowadzać nowe podejścia, takie jak terapie genowe i immunoterapia.
Dzięki zaawansowanej technologii i coraz lepszemu zrozumieniu biologii nowotworów, istnieje realna szansa na opracowanie skuteczniejszych metod leczenia, które mogą znacząco poprawić rokowania pacjentów. Warto również zwrócić uwagę na badania kliniczne, które będą prowadzone w nadchodzących latach, mające na celu ocenę skuteczności nowych terapii.
Podsumowując, badania nad glejakiem w 2024 roku wskazują na ekscytujące możliwości, które mogą zrewolucjonizować leczenie tego trudnego do zwalczenia nowotworu i dać nadzieję pacjentom oraz ich rodzinom.