Stwardnienie rozsiane to często wyniszczająca choroba autoimmunologiczna, która przynosi ze sobą szereg trudnych do zniesienia objawów, takich jak osłabienie mięśni, problemy z widzeniem, zaburzenia koordynacji oraz fizyczne odrętwienie. Obecnie, terapie koncentrują się głównie na łagodzeniu objawów, ale co jeśli moglibyśmy zmierzyć się z pierwotną przyczyną, która kryje się w naszym mózgu?
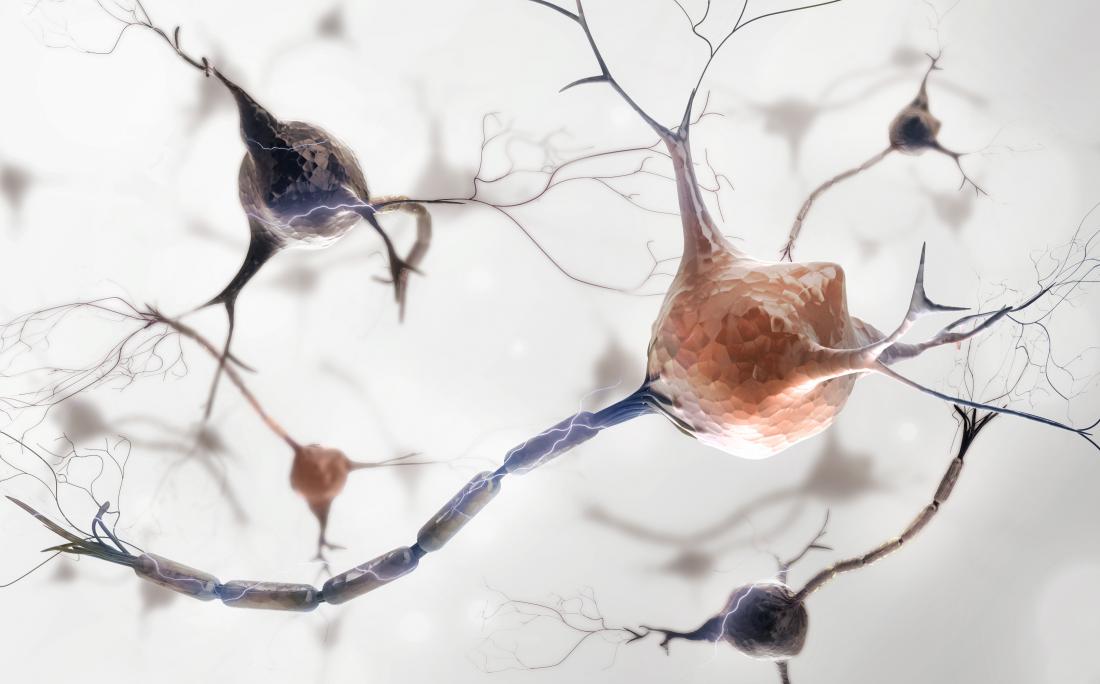
Choć podstawowe przyczyny stwardnienia rozsianego (SM) wciąż pozostają tajemnicą, wiadomo, że jednym z kluczowych czynników wywołujących objawy jest demielinizacja.
W trakcie tego procesu, układ odpornościowy atakuje i uszkadza mielinę, czyli «otoczkę» otaczającą aksony – długie wypustki, które łączą komórki nerwowe w mózgu oraz rdzeniu kręgowym.
Uszkodzenie mieliny prowadzi do zakłóceń w przesyłaniu sygnałów między komórkami nerwowymi, co skutkuje problemami z widzeniem, koordynacją oraz kontrolą mięśni. Dlatego kluczowym wyzwaniem dla badaczy zajmujących się SM jest wspieranie remielinizacji, czyli procesu tworzenia nowej «osłonki» mielinowej w sposób efektywny i skuteczny.
Według badania przeprowadzonego w 2016 roku, w Stanach Zjednoczonych żyje ponad 403.600 osób z SM, a wcześniejsze szacunki wskazują na około 2,3 miliona pacjentów na całym świecie.
Dr Veronique Miron z MS Society Edinburgh Center for MS Research w Wielkiej Brytanii oraz jej zespół dokonali przełomu w badaniach nad remielinizacją, odkrywając, że białko zwane activin-A odgrywa kluczową rolę w procesie naprawy mieliny.
Wówczas nie potrafili jeszcze zidentyfikować mechanizmu, dzięki któremu to białko zwiększa mielinizację. Jednak obecnie dr Miron i jej zespół odkryli, jak activin-A «włącza» proces naprawy.
Odkrycia badaczy zostały opublikowane w czasopiśmie
«Zachęcanie komórek do nowego mielin»
Dr Miron i jej współpracownicy badali mechanizm produkcji mieliny, w którym aktywina-A odgrywa kluczową rolę zarówno in vivo (w modelu myszy z SM), jak i in vitro (na ludzkiej tkance dostarczonej przez MS Society Tissue Bank).
Naukowcy zauważyli, że procesy prowadzące do produkcji mieliny zależały od ekspresji receptora aktywiny A znanego jako receptor 2a aktywiny (Acvr2a) na oligodendrocytach, które są komórkami zdolnymi do produkcji mieliny.
Analizując próbki tkanek pobrane od osób z postępującym SM, dr Miron i jej zespół odkryli, że poziomy Acvr2a były znacznie wyższe w tkankach, w których zachodziła remielinizacja. Natomiast w tkance pozbawionej jakichkolwiek oznak naprawy mieliny, poziomy Acvr2a były obniżone.
Badacze odkryli również, że aktywina-A wiąże się z Acvr2a, co sygnalizuje oligodendrocytom, aby rozpoczęły proces naprawy w miejscach, gdzie osłonka mielinowa aksonu została uszkodzona.
«Kiedy po raz pierwszy odkryliśmy białko aktywiny A,» wspomina dr Miron, «nie rozumieliśmy dokładnie jego roli w remielinizacji, teraz już wiemy, że wiąże się ono z określonym receptorem, co następnie prowadzi do aktywacji komórek odpowiedzialnych za naprawę mieliny.»
Remielinizacja odgrywa kluczową rolę w spowolnieniu postępu choroby oraz potencjalnym zatrzymaniu jej rozwoju, dlatego dr Miron podkreśla, że wyniki aktualnego badania mogą w końcu doprowadzić do nowego celu terapeutycznego dla leków.
«To naprawdę ekscytujące odkrycie, ponieważ możemy skoncentrować nasze wysiłki na opracowywaniu leków ukierunkowanych na ten receptor. Jeśli się to uda, możemy zachęcić komórki do tworzenia nowej mieliny w miejscach uszkodzeń związanych z SM.»
Dr Veronique Miron
Poniżej znajduje się film wideo, w którym dr Miron wyjaśnia znaczenie wyników badania w kontekście leczenia SM oraz jak mogą one wskazać drogę do skuteczniejszych terapii.
Nowe badania i perspektywy w terapii SM
W 2024 roku badania nad remielinizacją nabierają jeszcze większego tempa. Nowe terapie eksperymentalne, które koncentrują się na aktywacji Acvr2a, są obecnie w fazie prób klinicznych. Wstępne wyniki sugerują, że pacjenci mogą doświadczyć znaczącej poprawy w zakresie funkcji neurologicznych oraz jakości życia.
Dodatkowo, badania pokazują, że połączenie aktywiny-A z innymi czynnikami wzrostu może potęgować efekty remielinizacyjne. Więcej danych z badań klinicznych będzie dostępnych w nadchodzących miesiącach, co może prowadzić do rewolucyjnych zmian w terapii stwardnienia rozsianego.
Jak widać, perspektywy są obiecujące, a dalsze badania nad tym białkiem mogą otworzyć nowe możliwości w leczeniu SM, które do tej pory były nieosiągalne. W miarę jak naukowcy kontynuują badania, pacjenci mogą mieć nadzieję na lepsze i bardziej skuteczne terapie w przyszłości.